臨床
心臓カテーテル治療
心構造疾患
Structural Heart Disease
担当医師
林田 健太郎、金澤 英明、安西 淳、小平 真幸
従来、心臓カテーテル治療は主に冠動脈に対するものでしたが、近年では心構造疾患(SHD)に対するカテーテル治療が注目されています。当院では、肥大型閉塞性心筋症、慢性塞栓性肺高血圧症、心房中隔欠損症、動脈管開存症などに対するカテーテル治療を行っており、良好な成績を収めています。
特に注目すべき進歩としては、経カテーテル大動脈弁留置術(TAVI)があります。これは高齢者や合併症を持つ重度の大動脈弁狭窄症患者さんに対し、カテーテルを用いて生体弁を留置する方法で、予後の改善に寄与しています。当院では約1500例のTAVI治療を行い、2022年の周術期死亡率はゼロを達成しています。
また、開胸手術が困難な方や機能性僧帽弁閉鎖不全症などに対しての経皮的僧帽弁形成術(MitraClip)や抗凝固療法が困難な心房細動の方に経皮的左心耳閉鎖術(WATCHMAN)も当院では行っており、良好な成績を収めています。
これらの治療法は、「ハートチーム」の形成が重要であり、各分野のスペシャリストによるチーム医療により、「最も患者さんにやさしい」治療を提供しています。
経カテーテル大動脈弁留置術TAVIまたは経カテーテル大動脈弁留置術TAVR
重症の大動脈弁狭窄症で、開胸手術による治療が不可能または 非常に困難な患者さんに対する新しい治療です。大動脈弁をバルーンで拡張するだけでなく弁を留置する治療法です。
以前、重症大動脈弁狭窄症の治療のゴールドスタンダードは外科的な大動脈弁置換術でしたが、全患者の少なくとも30%は高齢または高リスクで、外科手術が出来ませんでした。これらの問題を克服するために、フランスのルーアン大学の循環器内科のAlain Cribier教授により、バルーンで大動脈弁を拡張するだけでなく、弁を留置する治療法が考案され、2002年に初めて施行されました。初期は未熟な治療で周術期死亡率も非常に高かったですが、デバイスの改良や経験・知識の蓄積により、年々安全性が向上し、現在は全ての重症大動脈弁狭窄症の患者さんにTAVI治療が選択肢の一つとして考えられるようになりました。
当院はカテーテル治療専門医、心臓外科専門医、イメージング専門医、心臓麻酔専門医などからなる強固な「ハートチーム」を持っています。1500件以上のケースを経験し、成功率は99.9%と非常に良好であり、安全かつ高品質なTAVIを提供しています。また、こうしたあらゆる手術リスクの患者さんにTAVI治療の適応が拡大したのみならず、最近では以下のような進歩があり、TAVI治療の適応の拡大がなされています。
外科生体弁劣化に対するTAVI治療
以前に外科的手術によって留置された生体弁が経年劣化し機能不全に陥った場合、TAVI治療によって人工弁機能不全を改善することが2018年7月より認可されました。再度の開胸手術をせずに行うことができ、多くの患者さんにとって、再手術よりもリスクの低い治療の提供が可能となっています。現在、外科生体弁劣化に対するTAVI治療ではSapien 3 UltraResiliaとEvolut FXという2種類のカテーテル弁の使用が認可されています。当院では双方の弁によるTAVI治療が実施可能であり、患者さんの状態に合わせて使い分けています。
人工透析中の方に対するTAVI治療
人工透析中の方は動脈硬化性疾患への罹患率が高いことが知られており、大動脈弁狭窄症を持つ方も少なくありませんでした。日本でも2021年1月にエドワーズライフサイエンス社製造のカテーテル弁でのTAVI治療が認可され、その後、日本メドトロニック社製造のカテーテル弁でのTAVI治療が2023年6月に認可されました。透析中の方のTAVI治療は非透析患者さんと比較すると合併症の発生率が高く、注意を要しますが、当院では2つの人工弁が使用可能であり、患者さんに応じて適切に使い分けを行い、安全なTAVI治療を心がけています。
カテーテル弁劣化に対するTAVI治療
外科生体弁同様、カテーテル弁もウシやブタの生体組織を用いて人工弁が製造されているため、術後に人工弁機能不全が生じることが懸念されていました。TAVI治療後10年間は、90%以上の方が人工弁への治療を要さずに経過することが報告されていますが、術後5年程度から機能不全が生じてくる可能性が指摘されており、日本でのTAVI治療開始から約10年経過した現在では、カテーテル弁の機能不全を呈する方がみられるようになりました。2023年9月現在、エドワーズライフサイエンス社製造のカテーテル弁の機能不全に対して、再度TAVI治療を行うことが可能となっており、当院でもカテーテル弁劣化をきたした方に再TAVI治療を実施しており、良好な成績が得られています。
当院では上記1~3全てのTAVI治療について施設認定がされており、大動脈弁に留置された生体弁が劣化してしまった方や透析治療中の方も当院でのTAVI治療を実施することが可能です。さらに、現在日本で使用可能なTAVI弁は3種類あり、当院では全てのTAVI弁を使用することが可能ですので、患者さんそれぞれにあった最適なTAVI弁を留置しています。
当院はカテーテル治療専門医、心臓外科専門医、イメージング専門医、心臓麻酔専門医などからなる強固な「ハートチーム」を持っています。1500件以上のケースを経験し、成功率は99.9%と非常に良好であり、安全かつ高品質なTAVIを提供しています。当院でのTAVI治療の詳細については下記のホームページをご覧ください。
TAVI
私たちは手技のみならず、世界にデータを発信していくことも目標として活動しています。
従来単施設研究では日常臨床に即した詳しいデータ収集は可能であるものの、症例数が少なく真実を得るための解析には足らない問題点がありました。しかし当院ではTAVIを中心に日本全国から症例が集まる非常に豊富な症例数を有する施設でもあり、長期的なフォローを行っていることで単施設の研究でも貴重なデータを世界へ発信しています。
また、当チーム責任者の林田医師はTAVIやMitraClipといったSHD関連の多施設レジストリーグループとしてのOCEAN-SHD研究会の代表を務めており、当チームのメンバーも本研究会に参加し、日本から世界の患者さんのためのデータを発信できるよう日々研鑽を積んでいます。
経皮的僧帽弁形成術(MitraClip)
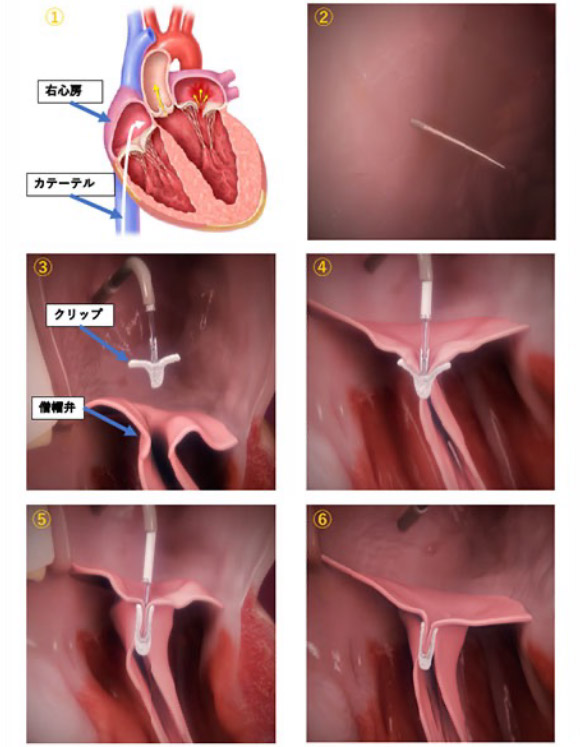
重症の僧帽弁閉鎖不全症になると、薬物療法だけでは心不全の症状(息切れや浮腫など)をコントロールすることが難しくなり、開胸して僧帽弁を人工弁に置換する手術や僧帽弁を形成する手術が必要となることがあります。しかし、開胸手術は身体への負担が大きく、高齢者や持病を抱えている方には困難な場合があります。そうした患者さんに対して、体への負担が比較的少ない僧帽弁接合不全修復システムによる経皮的僧帽弁形成術(MitraClip)が適用されることがあります。MitraClipは僧帽弁閉鎖不全症による血液の逆流を減らし、心不全の症状を改善する効果が期待できます。
このMitraClipデバイスを使用した僧帽弁閉鎖不全症に対する治療は左室機能低下に伴う僧帽弁閉鎖不全症に対して、従来の薬物治療に加えて、実施することで初めて心不全入院や死亡を回避することができることが証明された治療法です。当初2年間という比較的短い期間での有効性が発表されていましたが、近年、5年までの術後成績が報告され、5年後もMitraClipを用いた経皮的僧帽弁修復術を実施した患者さんでは、薬物治療単独に比較して心不全入院や死亡が少ないことが報告されました。この結果は従来に外科的治療では得られることができなかったものであり、非常に画期的な治療法であると考えられます。
当院では治験施設として早期からこの治療を開始し、良好な成績を収めています。また当初、日本で使用開始されたMitraClipは第2世代でありましたが、現在は第4世代までデバイスの進歩が得られ、以前は単一のサイズしかなかったクリップが、サイズの異なる4種類のクリップを選択可能となりました。これにより、より少ないクリップ数で僧帽弁閉鎖不全症が制御できることが報告されており、手技時間の短縮につながり、患者さんの負担をさらに軽減されることが期待されています。当院でも最新世代のMitraClipによる治療は可能であり、すでに4種類全てのクリップの使用経験もあることから、ハートチームで協議して、患者さんに最適なクリップを選択することで良好な手術成績を収めています。当院でのMitraClipを使用した治療の詳細については下記のホームページをご覧ください。
MitraClip
左心耳閉鎖 LAAC
心房細動の患者さんでは心臓内に血栓が形成され、それが血流に乗って、細い血管で詰まってしまうこと(血栓塞栓症)が生じることが知られています。
こうした脳卒中などを起こしうる血栓塞栓症の原因である血栓の90%以上が心臓内の左心耳(LAA)という部位から発生していることが知られています。
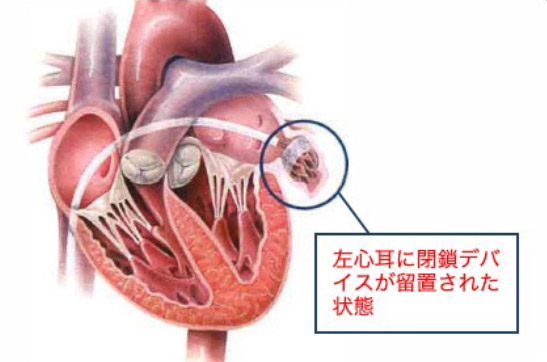
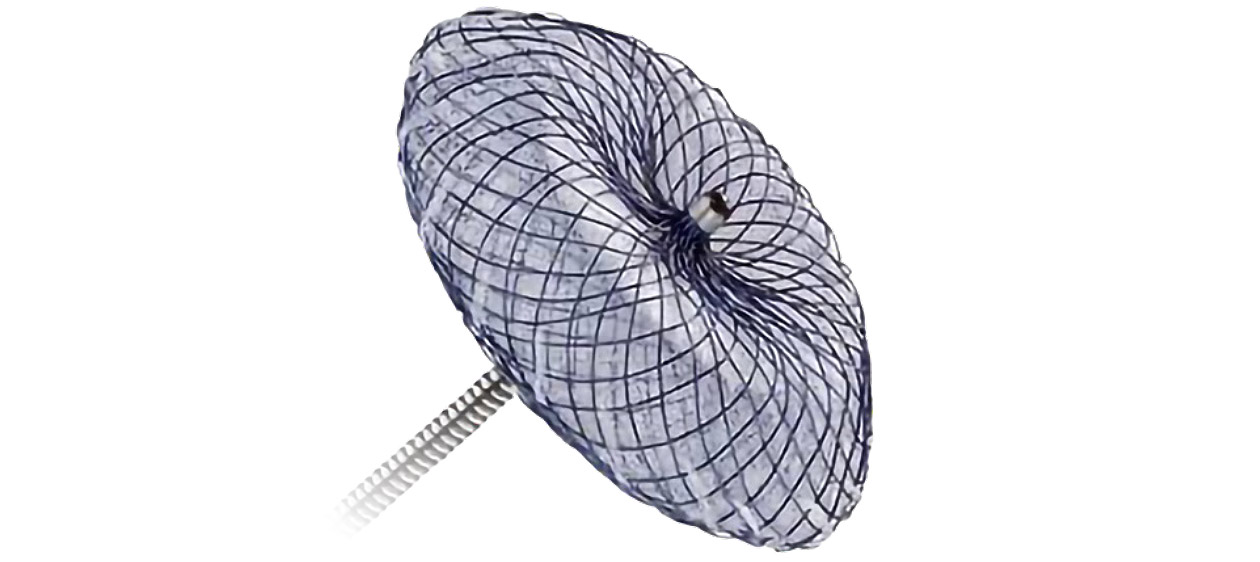
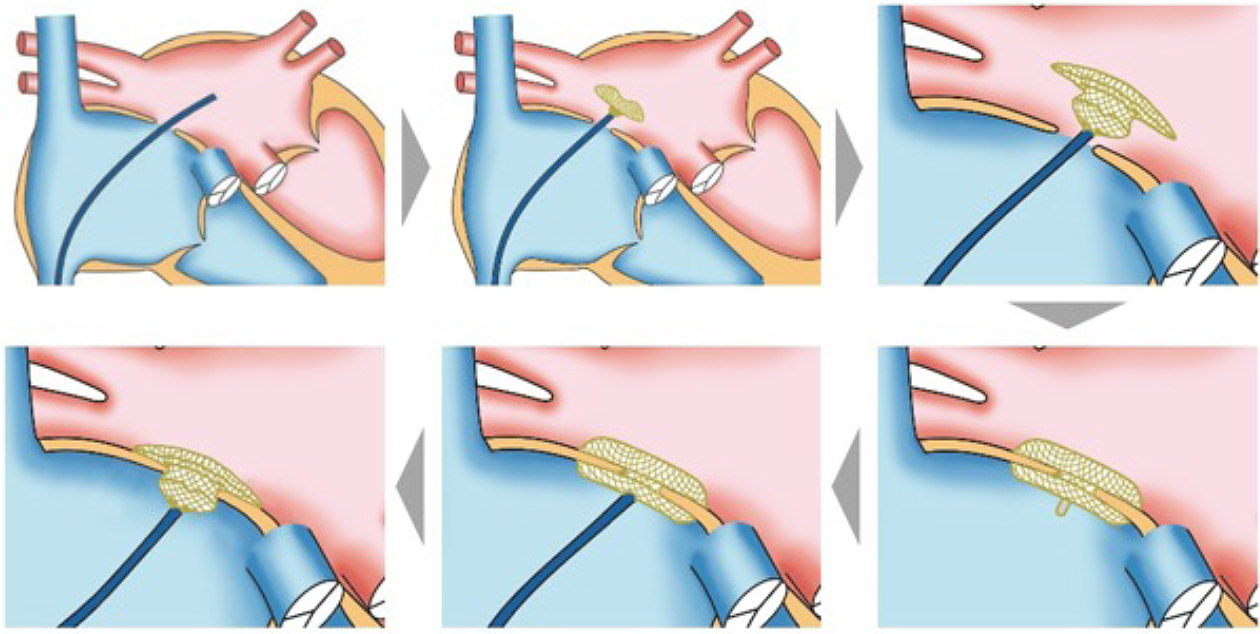
経カテーテル左心耳閉鎖術のデバイスを心臓の左心耳(LAA)に留置することで永久に閉鎖し、血栓が全身に飛ぶのを防ぎ、脳卒中リスクを減らすことができます。
また、こうした血栓塞栓症を防ぐために抗凝固薬を使用することが多いですが、抗凝固薬は脳出血などの重大な合併症を引き起こしえます。経カテーテル左心耳閉鎖術を行うと抗凝固療法を中止できる可能性もあります。
左心耳閉鎖術後は抗血小板剤の内服が必要になりますが、抗血栓療法であっても抗凝固薬の方が出血のリスクが上がるのではないかという報告があり、実際に経カテーテル左心耳閉鎖術後の方とカテーテル治療をせずに従来通りの心房細動に対する抗凝固療法を継続した方とでは、手技に関連するもの以外の出血が抗凝固療法を継続した方では多かったとする報告があります。
このように血栓の発生部位である左心耳を閉鎖することで、抗凝固療法を行なっても脳梗塞を発症されてしまった方のみならず、抗凝固療法による出血合併症に悩まされている方にも、この経カテーテル左心耳閉鎖術は非常に良い治療であると考えらます。
また日本で使用されている左心耳閉鎖デバイスであるWatchmanデバイスは近年従来のWatchman2.5からWatchman FLXに改良されました。
この新しいWatchman FLXデバイスは従来のものと同様に安全に使用可能であり、尚且つ、以前のデバイスと比較して良好な左心耳閉鎖、デバイス自体への血栓の付着が少ないことが報告されました。
また近年報告されたメタ解析でも同様にWatchman FLXは以前のWatchman 2.5と比較して合併症が少ないなどの優越性が報告されています。
当院でも最新Watchman FLXを用いて、経カテーテル左心耳閉鎖術を行っており、非常に良好な成績を収めています。
当院での経カテーテル左心耳閉鎖治療の詳細については下記のホームページをご覧ください。
WATCHMAN
経皮的僧帽弁裂開術 PTMC
症状や心房細動の出現、または心臓内に血栓が形成された場合、カテーテル(細い管)による治療や外科的な心臓手術が必要となります。カテーテルによる治療法は心臓内に血栓がないこと、僧帽弁逆流症が重度でないことが前提で、弁の硬さなどを総合的に判断して治療が行われます。この治療法は経皮経静脈的僧帽弁交連裂開術(PTMC)と呼ばれます。
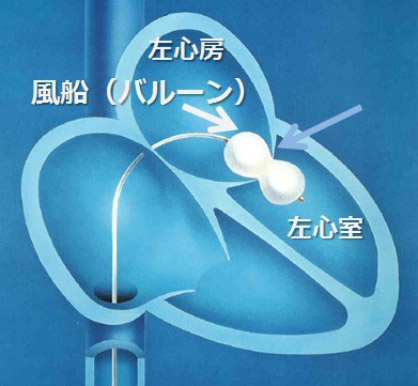
カテーテルを用いて足の動脈から直接心臓に到達し、硬くなった弁にイノウエ・バルーンという風船を運び、そこでバルーンを広げて、硬くなった僧帽弁を広げる治療です。心臓手術に比べ開胸術ではないので、患者さんの負担は少ないですが、治療が安全に行えるかどうか、慎重に吟味する必要があります。
卵円孔開存PFO閉鎖術
卵円孔開存は、右心房と左心房の壁に開いている孔で、成人の2〜3割に見られます。通常は問題とならないですが、稀に脳梗塞や一過性脳虚血発作の原因となることがあります。
対象となるのは以下のような方々です
卵円孔開存の関与があり得る潜因性脳梗塞の診断基準に合致した患者さん
適切に施行された抗血栓療法中に上記潜因性脳梗塞を発症した方
原則として、60 歳未満の方
(女性の場合)妊娠していない、かつ 1 年以内の妊娠を希望しない方
治療は基本的に局所麻酔を使い、カテーテルを太ももの付け根の静脈から挿入し、心臓まで卵円孔の閉鎖に使用する閉鎖栓を運びます。治療後は一定時間ベッド上で安静後、翌日から歩くことが可能です。経過が順調であれば数日後に退院可能です。
担当外来
小平 真幸(月曜午後、金曜午前)、木村 舞(火曜午後)
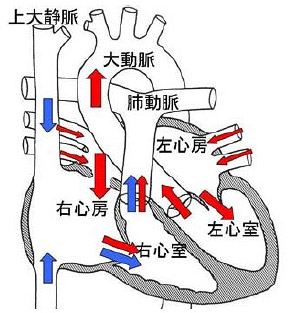
心房中隔欠損症 ASD
心房中隔欠損症とは、左心房と右心房の間の壁(中隔)に穴(欠損孔)があいている病気です。左心房から右心房への血液の漏れが生じますが、多くの場合には症状はなく、乳幼児健診や学校心臓検診で心臓の雑音や心電図の異常から発見されます。欠損孔を介して左心房から右心房に流れる血液の量(短絡量=心臓への負担)を心エコー検査や心臓カテーテル検査で詳しく調べ、欠損孔の閉鎖が必要かどうか(=治療適応)が決まります。欠損孔の閉鎖が必要な場合、二次孔型心房中隔欠損症については、閉鎖栓デバイスを用いたカテーテルによる治療が一般的となってきています。
欠損孔の場所によっては、人工心肺を用いた外科的閉鎖術の適応になりますし、静脈洞型や冠静脈洞型では原則手術で治療することになります。
肺高血圧合併例では、肺高血圧専門医(平出医師)と協力して診療しています。肺血管拡張薬による治療を最初に開始して肺動脈圧を下げてから心房中隔欠損孔を閉鎖するtreat and repairも症例を選択して実施しています。
担当外来
小平 真幸(月曜午後、金曜午前)、木村 舞(火曜午後)
動脈管開存症 PDA
動脈管とは、胎児期において大動脈と肺動脈をつなぐ小さな管で、新鮮な血液を全身に流すために必要です。しかし、生まれた後は肺が働き始めるため動脈管は不要となり、通常は生後48時間以内にほとんど血液が流れなくなり、数週間で完全に閉じます。動脈管開存とは、生後も動脈管が開いたままの状態を指します。大動脈から肺動脈へ血液が漏れることで心臓に負担がかかります。治療法としては、開胸手術とカテーテル治療の2つがあります。手術では動脈管を糸で結び、カテーテルではコイルやアンプラッツアー閉鎖栓を用いて塞ぎます。大人の患者さんでは、動脈管が硬くなっていることが多いため、カテーテル治療が一般的です。
担当外来
小平 真幸(月曜午後、金曜午前)、木村 舞(火曜午後)
バルーン肺動脈形成術(BPA)
担当医師
安西 淳
慢性肺血栓塞栓性肺高血圧症(CTEPH:Chronic ThromboEmbolic Pulmonary Hypertension)に対するバルーン肺動脈形成術(BPA)は、低侵襲で入院期間が短く、有効性も高い優れた治療です。実施に際して、経験のある専門医が外科的肺動脈内膜摘除術や薬物療法(肺血管拡張薬)と合わせて総合的に検討することが重要です。
当科では火曜日午後の外来(担当医 安西 淳)にてカテーテル治療を含めたCTEPHの治療に関してマネージメントさせていただきます。本疾患および治療でお悩みの患者さん・ご家族がおられましたら、お気軽にご相談ください。
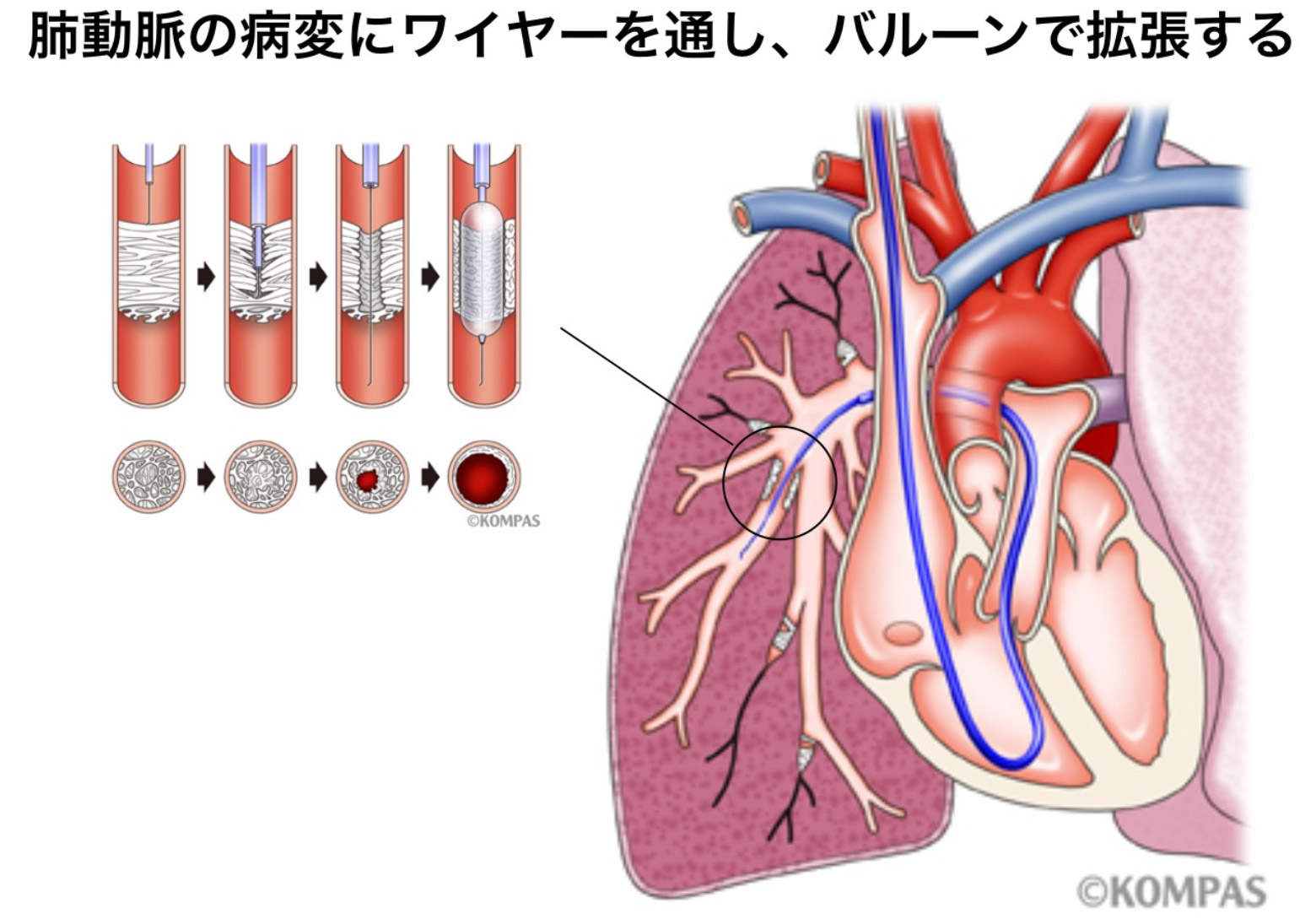
バルーン肺動脈形成術
(BPA: Balloon Pulmonary Angioplasty)
慢性肺血栓塞栓性肺高血圧症(CTEPH)は、器質化(古い)血栓が肺動脈を慢性的に狭窄・閉塞する病気です。広範囲の肺動脈が狭窄・閉塞すると、肺動脈圧が上昇して右心不全を発症します。早期に適切な治療を受けなければ、生命に関わるといわれ、国が難病認定している病気です。肺動脈の近位に血栓がある中枢型CTEPHの場合、外科的に血栓を摘出する肺動脈内膜剥離術(PEA)の施行が望ましいです。そして、肺動脈の末梢に血栓がある末梢型CTEPHでは一般的に外科手術が困難といわれています。加えて、年齢やほかの合併疾患のために全ての患者さんがPEAの対象にならないといわれています。
近年、肺動脈の狭窄・閉塞をバルーンで拡張するカテーテル治療(バルーン肺動脈形成術:BPA)が有効であることが多く報告されています。治療対象となる肺血管は左右で18本存在するために、BPAは複数回、実施しなければなりません。外科治療と比較して、末梢型や外科手術困難症例に対して実施することができます。有効性が報告されているBPAではありますが、新しい治療であり、治療効果や治療後の経過など、十分な経過観察が必要です。当院では、BPAの短期・長期の有効性について検証しながら、慎重に治療を進めています。
慢性肺血栓塞栓性肺高血圧症(CTEPH)の治療法
薬物療法は治療の基本であり、多くの患者さんの症状を軽快することができます。しかし、病気は進行性であり、早い段階で治療専門医が外科手術またはカテーテル治療が必要なのかを検討するべきだと考えます。必要であれば、早期に治療を受けるのが望ましいと考えます。なぜなら、進行してからでは治療が困難になるからです。当院は、患者さんがどのような治療法を希望されているのか、どの治療法が一番良いのかを十分に検討して治療方針を決定していきます。当院では、外科手術・カテーテル治療の双方の術者と相談することができます。
薬物療法・在宅酸素療法
抗凝固薬(ワーファリンなど)、利尿薬、肺血管拡張剤は治療の基本であり、多くの患者さんの症状を軽くできます。しかし、本疾患は進行性で薬物療法のみでは十分な治療効果が得られない場合も多く、注意深い経過観察が必要です。なお、酸素飽和度が低くなる低酸素血症に対しては在宅酸素療法も行われます。
外科的肺動脈内膜摘除術(PEA)
全身麻酔下で胸骨正中切開を行い、外科的に古い血栓を取り出す根治術です。肺動脈の近い部分に血栓が存在する中枢型の患者さんには効果的な治療です。しかし、肺動脈の末梢に血栓がある末梢型の場合には外科的な血栓除去が困難であるといわれています。
バルーン肺動脈形成術(BPA)
局所麻酔下で行う低侵襲性のカテーテル治療です。中枢型のCTEPHに加えて、 高齢者、全身麻酔が困難な場合、末梢型CTEPHに対しても治療することができます。複数回の治療によりかなりの改善効果を得ることができます。
当院のBPAの実際
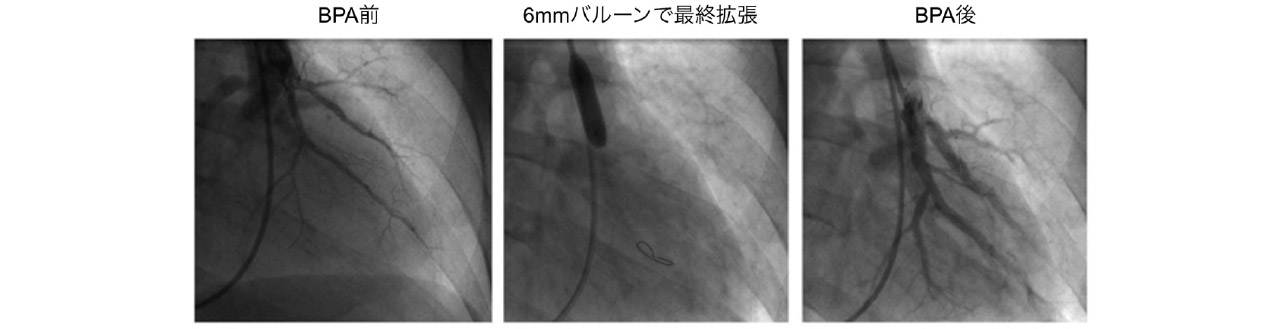
通常、局所麻酔を行った上で、大腿静脈あるいは内頸静脈からシースという管を挿入します。シースからカテーテルを入れて肺動脈の病変近くまで進めます。カテーテルで肺動脈を直接造影し、狭窄・閉塞病変を詳細に確認します。確認後、狭い部分に細いガイドワイヤーを進めて、血管造影、血管内超音波(IVUS)、光干渉断層法(OCT)などで肺動脈病変の状態や血管の太さを確認します(閉塞の場合、かなり固いガイドワイヤーを必要とすることがあります)。確認後、バルーンで狭い病変を拡張します(図1、図2)。繰り返し同様に複数の病変をバルーンで拡張するため、BPAは平均1時間30分程度かかります。
個人差はありますが、術後、3~5日で退院することが多いです。
BPAにより肺高血圧の改善後、定期的に右心カテーテル、肺動脈造影を行い、治療の効果を評価していきます。
BPAの治療成績
2001年、米国のFeinsteinらの初期報告では、周術期死亡率は11.1%、術後肺障害発生率は61%とかなり難易度の高い手術でした。2000年半ばより、日本でも外科手術適応外であるCTEPH(inoperable CTEPH)に対して、徐々にBPAが実施されるようになり、大きく安全性と有効性が改善してきました。
当院では2012年11月から2017年9月で、計123名がBPA治療を終了しています。
当院でのBPA治療における患者背景は、年齢は63.4±13.9歳、女性は65%、WHO機能分類IIIおよびIV度は78%、BPA平均手技回数は6.4±2.1回で、BPAにより平均肺動脈圧は37.4±10.2mmHgから19.5±4.1mmHg、肺血管抵抗746±597dyne・sec・cm-5から 279±121dyne・sec・cm-5、心拍出量は3.8±1.4L/minから3.9±1.1L/min、右房圧は6.3±3.5mmHgから1.9±1.7mmHgへ改善していました。また、6分間歩行距離も治療終了6カ月後に334±110mから442±95mへ改善しました。なお、BPA関連合併症においては、47セッション(6.0%)で血痰、6セッション(0.8%)で非侵襲的陽圧換気(NPPV)を装着しました。なお、死亡症例や人工心肺装着を必要とした症例はありませんでした。
近年、治療成績の向上に加えて、BPA手技関連肺障害に対する止血術が確立し、カテーテル治療デバイスが進歩しています。引き続き、当院ではBPAに際して、CT、SPECT、IVUSなどの画像技術を積極的に活用し、さらなる治療成績の向上に役立てています。
経皮的中隔心筋焼灼術 PTSMA
経皮的中隔心筋焼灼術
(PTSMA:Percutaneous transluminal septal myocardial ablation)
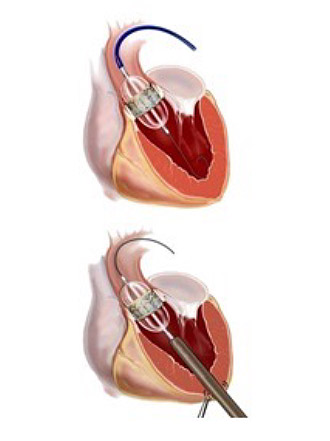
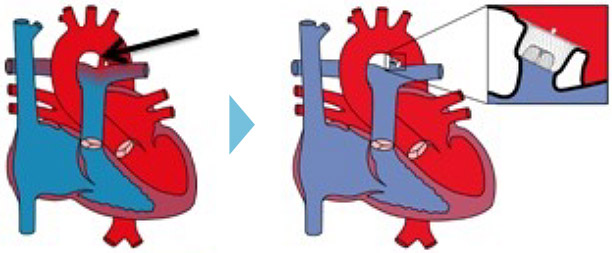
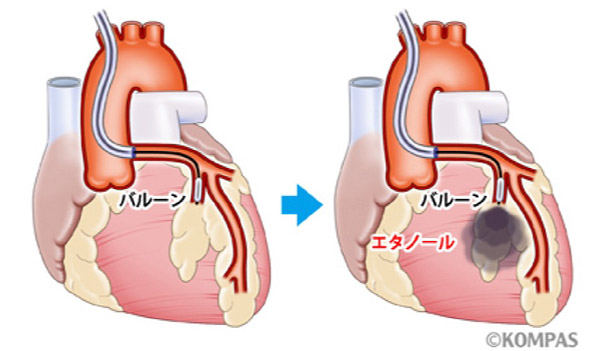
症状のある、薬物治療抵抗性の閉塞性肥大型心筋症に対して、カテーテルを使用して純エタノールにより閉塞責任中隔心筋を焼灼壊死させる治療法のことです。経皮的中隔心筋焼灼術(PTSMA)は1995年より欧州にて始まり、薬物治療無効例に対し、外科的に肥大心筋を切除する中隔心筋切除術の代替治療として位置づけられる治療法です。治療の仕組みは、左心室の出口(流出路)を圧排する肥大心筋に流れる冠動脈左前下行枝の枝である中隔枝にエタノールを極少量注入して、肥大心筋を焼灼し、薄くすることによって左室内圧較差を減らす治療法です(図1)。
外科手術を受けることができる全身状態であれば外科的な中隔心筋切除術が第一選択となりますが、本治療の最大の特徴は、「低侵襲性」(体力の消耗や傷口が小さい)です。症状をはじめ、僧帽弁逆流や不整脈合併の有無などを総合的に判断し、よくご相談させていただいた上で治療方針を決定しています。他院からご紹介いただくケースで、薬物療法を変更あるいは強化すると症状が改善するケースも少なくありません。
当院での経皮的中隔心筋焼灼術
カテーテル治療担当医が、心臓エコー担当医師の立ち会いの下、治療を行っています。術中の正確な心臓エコー所見の解釈が、治療の成否に関わりますので、心臓エコー専門医の見解を術中に聞く事が出来る状態で治療を行えるのは当院の強みと考えています。カテーテル治療は基本的には局所麻酔で行い、治療に要する時間は2時間強です。当院では、治療を行う前に、事前に検査入院をしていただいている関係上、治療当日は事前の検査結果を参考に治療を行っています。治療にともなう入院期間は1週間強です。
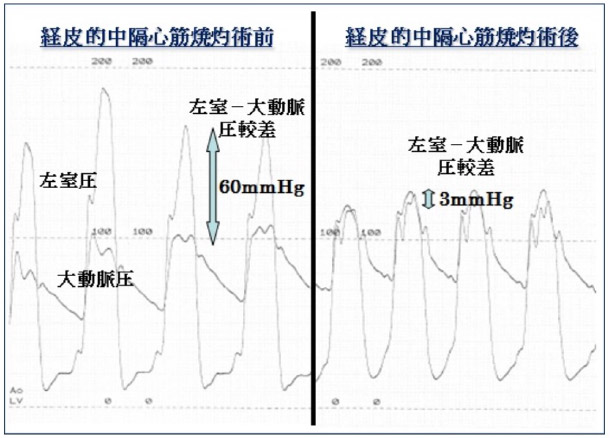
カテーテル治療の成否は、治療終了時の左心室と大動脈の圧較差で判定します(圧較差:左心室から大動脈への血液の通りやすさを反映します。安静時に圧較差が30mmHg以上あれば“閉塞性”と判断します。値が大きいほど、血液が通りにくく、病気の程度は重症と判断します。カテーテル治療後は治療が成功した患者さんでは圧較差は10mmHg以内にまで減少します。(図2)。カテーテル治療後は、閉塞性肥大型心筋症外来にて、心臓超音波、心臓MRIおよび心肺運動負荷試験などを施行させていただき、治療効果の判定および評価を行います。
当科では火曜日午前の外来(担当医 安西 淳)にてカテーテル治療を含めた閉塞性肥大型心筋症の治療に関してマネージメントさせていただきます。
心臓カテーテル治療外来について